arme14
Usuario (Argentina)

.1. Comer una bolsa de frituras al día es equivalente a beber cinco litros de aceite de cocina al año. 2 Europa tiene un país cuya religión oficial es el budismo: la república de Kalmukia. 3. Las balas no pueden penetrar más de dos metros en el agua [con impulso suficiente para hacer daño, claro]. 4. Más del 90% de los accidentes aéreos tienen supervivientes. 5. Para dar un beso, el doble de personas inclina su cabeza a la derecha en vez de a la izquierda. 6. Los dirigibles usan tanto combustible en una semana como un 767 usa para moverse desde el andén hasta la pista. 7. Los padres tienden a determinar (genéticamente) la estatura de los hijos; las madres, el peso. 8. Hay 200 millones de blogs abandonados en la Internet, que ya no se actualizan. 9. El disfraz de león en el filme El Mago de Oz estaba hecho con leones auténticos. 10. La nariz humana, presionada contra el suelo como la de un perro, es lo bastante sensible para seguir un rastro en terreno abierto.
Explosivos: Son compuestos o mezclas de compuestos químicos que arden o se descomponen rápidamente generando grandes cantidades de gas y calor, y los consiguientes efectos de presión repentinos. En tiempos de paz los explosivos se utilizan principalmente para voladuras en minería y en cantería, aunque también se emplean en fuegos artificiales, en aparatos de señalización y para hacer remaches y moldear metales. Los explosivos se utilizan también como propulsores para proyectiles y cohetes, como cargas explosivas para la demolición, y para hacer bombas y minas. El primer explosivo conocido fue la pólvora, llamada también “polvo negro”. Se empezó a utilizar hacia el siglo XIII y fue el único explosivo conocido durante siglos. Los nitratos de celulosa y la nitroglicerina, ambos descubiertos en 1846, fueron los primeros explosivos modernos. Desde entonces, nitratos, compuestos de nitrógeno, fulminatos y azidas han sido los principales compuestos explosivos utilizados por separado o mezclados con combustibles y otros agentes. El trióxido de xenón, que fue el primer óxido explosivo, se desarrolló en 1962. La Pólvora: La pólvora, es un polvo explosivo utilizado en balística, en particular pólvora negra, una mezcla explosiva de un 75% de nitrato potásico, un 15% de carbón y un 10% de azufre aproximadamente. La pólvora fue el primer explosivo conocido; su fórmula aparece ya en el siglo XIII, en los escritos del monje inglés Roger Bacon, aunque parece haber sido descubierta por los chinos, que la utilizaron con anterioridad en la fabricación de fuegos artificiales. Es probable que la pólvora se introdujera en Europa procedente del Oriente Próximo. Berthold Schwarz, un monje alemán, a comienzos del siglo XIV, puede haber sido el primero en utilizar la pólvora para impulsar un proyectil. Sean cuales sean los datos precisos y las identidades de sus descubridores y primeros usuarios, lo cierto es que la pólvora se fabricaba en Inglaterra en 1334 y que en 1340 Alemania contaba con instalaciones para su fabricación. El primer intento de utilización de la pólvora para minar los muros de las fortificaciones se llevó a cabo durante el sitio de Pisa en 1403. En la segunda mitad del siglo XVI, la fabricación de pólvora en la mayoría de los países era un monopolio del Estado, que reglamentó su uso a comienzos del siglo XVII. Fue el único explosivo conocido hasta el descubrimiento del denominado oro fulminante, un poderoso explosivo utilizado por primera vez en 1628 durante las contiendas bélicas que se desarrollaron en el continente europeo. UN POCO DE HISTORIA Por Raquel Cubero Aunque su función primigenia era la de servir de vía para la introducción en Europa de sedas y telas orientales, muchos otros objetos y materiales acabaron por llegar a occidente a través de ella. Entre ellos se encontraba uno que cambiaría el curso de la historia: la pólvora. La pólvora, el primer explosivo conocido, fue descubierta por casualidad en China en torno al siglo IX. Su hallazgo parece ser fruto de las investigaciones de algún alquimista que, en su búsqueda del elixir de la eterna juventud, dio por accidente con la fórmula del explosivo. De hecho las primeras referencias a la pólvora las encontramos en textos herméticos advirtiendo de los peligros de mezclar determinadas sustancias. En el siglo X ya se utilizaba con propósitos militares en forma de cohetes y bombas explosivas lanzadas desde catapultas. Se sabe que ya en el año 1126 se utilizaban cañones hechos de tubos de bambú para lanzar proyectiles al enemigo. Más tarde esos tubos serían sustituidos por otros de metal más resistente; el más antiguo del que se tiene noticia data de1290. Desde China el uso militar de la pólvora pasó a Japón y a Europa. Se sabe que fue usado por los mongoles contra los húngaros en 1241 y que Roger Bacon hace una mención en 1248. Hasta ese momento Europa sólo había contado con un producto inflamable llamado "fuego griego" que sin embargo no podría competir con la efectividad del recién llegado invento. Durante el siglo XIV el uso de cañones se generalizó tanto en China como en Europa, pero el problema seguía residiendo en crear tubos de metal capaces de contener las tremendas explosiones que se producían en su interior. Este problema pudo haber conducido a la falsa afirmación de que los chinos sólo utilizaron la pólvora para hacer fuegos artificiales, lo que no es en absoluto cierto ya que está documentado que hicieron uso de ella con propósitos bélicos en numerosas ocasiones. Así por ejemplo el grosor y la solidez de las murallas de Beijing deja bien a las claras que se diseñaron para resistir el ataque de la artillería enemiga y la dinastía Ming cambió la ubicación de la antigua capital Nanjing por el hecho de que las colinas de alrededor eran una localización demasiado tentadora para que el adversario ubicara sus cañones. Cuenta la leyenda que la fórmula pudo llegar a Europa en 1324 de la mano de un monje peregrino. La receta consistía en la mezcla de carbón, azufre y salitre que el religioso comunicó al abad de un monasterio donde pernoctó. A la mañana siguiente el monje que se encontraba en la puerta al ver salir al huésped, pudo comprobar con horror que debajo de los ropajes monacales le asomaba un rabo peludo: era el mismísimo diablo que el terrible invento venía a perturbar para siempre y a sembrar el caos la sociedad de la época. La pólvora se extendió con rapidez por toda Europa y jugó un papel fundamental en el equilibrio de poder que se establecería a partir de entonces, ya que eran muy pocos los personajes que contaban con dinero y capacidad suficiente para fabricar armas. Entre los siglos XV al XVII se asistiría a un amplio desarrollo de la tecnología relacionada con al pólvora. Los avances en el campo de la metalurgia hicieron posible la elaboración de armas de pequeños tamaño y mosquetes. Resulta curioso que todavía en el siglo XV, Enrique VIII de Inglaterra manifestara que "las armas de fuego nunca suplantarían al arco largo de la infantería inglesa". Incluso tiempo después, cuando las armas se habían generalizado en todos los ejércitos, muchos seguían considerando su uso como una vileza impropia de verdaderos caballeros. A partir de la segunda mitad del siglo XVI la fabricación de la pólvora en casi todos los países, estaba ya en manos del Estado y su uso sería reglamentado poco después. En 1886 Paul Vielle inventó un tipo de pólvora sin humo hecho con nitrocelulosa gelatinizada mezclada con éter y alcohol. Esta mezcla se pasaba por unos rodillos para formar finas hojas que después se cortaban con una guillotina al tamaño deseado. El ejército francés fue el primero en usar este nuevo tipo de explosivo, que no formaba humo y era mucho más potente que el anterior, y otros países europeos no tardaron es seguir su ejemplo. Muchas otras innovaciones se sucedieron en el campo de los materiales explosivos hasta llegar a la actualidad, pero sin duda la aparición de la pólvora en occidente en la Edad Media fue el acontecimiento más significativo.
El Ministerio de Salud desaconsejó su uso por los riesgos para la salud. Igual, no las prohibirá . El Ministerio de Salud de la Nación y las dos entidades médicas relacionadas con la dermatología salieron ayer a desaconsejar el uso de las camas solares para broncearse, particularmente en personas menores de 35 años. Si bien no prohibirán esas camillas con radiación ultravioleta, enfatizarán en que la gente deje de concurrir a los locales. El 31 de octubre, Clarín había publicado que las sociedades médicas venían reclamando un mayor control para los 500 locales que ofrecen el servicio del bronceado artificial en el país. Es que la mayoría no informa sobre los riesgos que las camas solares tienen para la salud. Días después, funcionarios de tres dependencias del Ministerio de Salud de la Nación, a cargo de Juan Manzur, se reunieron con los titulares de la Sociedad Argentina de Dermatología y la Asociación Argentina de Dermatología. En el encuentro analizaron estudios publicados y la advertencia que en julio de 2009 había hecho la Agencia Internacional para la Investigación sobre el Cáncer, que depende de la Organización Mundial de la Salud (OMS), que confirmó que los rayos ultravioletas que emiten las máquinas son “definitivamente cancerígenos” . “Hay muchas evidencias científicas que demuestran los riesgos que acarrea la exposición en las camas solares: aumenta el riesgo de padecer cáncer de piel, cataratas en los ojos, envejecimiento prematuro, y deficiencias en el sistema de defensas del organismo. Por estas razones, consideramos que hay que desalentar el uso de las camas solares”, dijo a Clarín Roberto Pradier, director del Instituto Nacional del Cáncer, que depende del Ministerio de Salud. El funcionario aclaró que en lugar de preparar la piel para el verano las dosis de rayos ultravioletas artificiales se acumulan y refuerzan el efecto cancerígeno . Pero aclaró que no se decidirá la prohibición porque la habilitación de los locales con camas solares está a cargo de cada distrito. “Veníamos reclamando incluso desde antes de que la OMS diera la advertencia, porque sabemos los perjuicios”, recordó Graciela Ferraro, presidenta de la Asociación Argentina de Dermatología. “En los locales debería haber un profesional que evalúe si cada cliente puede o no exponerse. Esperamos que ahora la gente sea más conciente de los riesgos y que no vaya”, agregó la dermatóloga. El uso de las camas solares empezó en 1985 en la Argentina. Con la crisis de 2001 bajó la concurrencia, pero durante los últimos años la actividad repuntó . En 2006 se había prohibido el ingreso de menores. ¿Por qué la gente sigue yendo a las camas solares? “Porque forma parte de una filosofía de vida que cree que parecer es más importante que ser –opinó Ferraro–. Pero la cama solar tiene un alto costo para la salud . La cuestión que los efectos se ven en 10 o 15 años, con los cánceres de piel. Y la gente no piensa a tan largo plazo cuando decide ir a las camas solares. Hay adictos al bronceado ”. Fuente: http://www.clarin.com/sociedad/salud/Camas-solares-advertencia-oficial_0_381561972.html
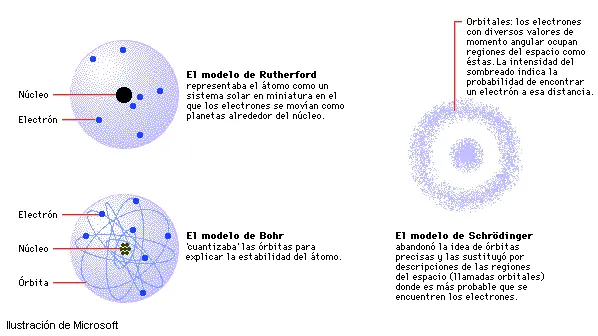
El presente trabajo trata de "La Evolución Histórica del Modelo Atómico". Muchos de los procesos químicos que ocurren, tanto en la naturaleza v como en los laboratorios, tienen una explicación a nivel microscópico, donde átomos y moléculas participan activamente. Así, para comprender los fenómenos y dar una explicación que se aproxime a la realidad de lo que sucede, los científicos utilizan modelos. Un modelo explica el fenómeno por medio de una analogía que permite visualizar o hacer una creación mental cuando lo ocurrido no se presenta explícitamente a nuestros sentidos. Por lo general el modelo constituye una explicación sencilla, y proporciona una semejanza estructural con el fenómeno que se estudia. Un modelo no es una estructura rígida, sino que puede perfeccionarse, cambiarse o desecharse si se vuelve obsoleto y ya no cumple la función para la cual fue propuesto. Desde que la ciencia dio sus primero pasos y los químicos iniciaron el estudio de la composición y propiedades de la materia, y se desarrolló de la teoría atómica, los científicos emplearon modelos para comprender la naturaleza del átomo. En la actualidad se acepta que la materia está formada por átomos y se tiene un modelo atómico consistente con el cual se explica satisfactoriamente su comportamiento. Sin embargo, para llegar a este modelo, para que se llegará a concebir el átomo en su forma actual, pasó mucho tiempo y fueron muchos los científicos que investigaron; plantearon teorías y crearon modelos respecto a la estructura de la materia y del átomo en sí. A pesar de las dificultades evidentes, el concepto de que la materia es de naturaleza corpuscular (formada por partículas) ha llegado a ser uno de los postulados fundamentales y fructíferos de la Química y merece la pena revisar algunos pasos importantes dados para llegar a esta conclusión. A continuación se presentan los modelos atómicos más importantes desde Dalton a la actualidad. Evolución Histórica del Modelo Atómico Modelo Atómico de John Dalton: John Dalton, profesor y químico británico, estaba fascinado por el rompecabezas de los elementos. A principios del siglo XIX estudió la forma en que los diversos elementos se combinan entre sí para formar compuestos químicos. Aunque muchos otros científicos, empezando por los antiguos griegos, habían afirmado ya que las unidades más pequeñas de una sustancia eran los átomos, se considera a Dalton como una de las figuras más significativas de la teoría atómica porque la convirtió en algo cuantitativo. Dalton desarrolló un modelo científico y formulo una serie de postulados concernientes a la naturaleza de los átomos, los cuales destacaban la masa como una propiedad atómica fundamental. Basándose en los datos experimentales imperfectos de que disponía, Dalton propuso su teoría por medio de los siguientes postulados: 1. La materia está compuesta por partículas pequeñísimas llamadas átomos. 2. Los átomos son individuales y no pueden transformarse unos en otros. 3. No pueden ser creados ni destruidos. 4. Los elementos se hallan constituidos por átomos. Los átomos de un mismo elemento son idénticos en tamaño, forma, masa y todas las demás cualidades, pero diferentes a los átomos de los otros elementos. 5. Los átomos de unen para formar las moléculas, combinándose en proporciones fijas de números enteros y pequeños. Por ejemplo, un átomo de azufre (S) se combina con dos átomos de oxígeno (O) para formar la molécula SO2, y lo hacen siempre en la relación de 1:2. 6. Dos o más elementos, pueden combinarse de diferentes manera para formar más de una clase de compuestos. Así, entre el azufre (S) y el oxígeno (O) se pueden formar dos compuestos diferentes, el SO2 y el CO2. En cada uno de estos compuestos hay una proporción de átomos y masa diferente pero definida y siempre en la relación de números enteros y pequeños. Durante casi un siglo no se dudó de ninguno de los puntos esenciales de la teoría atómica propuesta por Dalton. Modelo Atómico de John Thomson: Para los científicos de 1900, al tomar como base los experimentos con rayos catódicos, rayos positivos y, en general, la relación entre materia y electricidad, era clara la necesidad de revisar el modelo atómico propuesto por Dalton. El descubrimiento del electrón realizado por John Thomson, físico británico, así como los llamados rayos canales o rayos positivos, que pueden observarse como un fino haz de luz detrás de un tubo de descarga con el cátodo perforado, llevó a la conclusión de que el átomo no podía ser una esfera rígida de material característico para cada elemento, como había supuesto ingenuamente Dalton, sino que debía poseer una estructura. Aunque el nuevo modelo atómico explicaba la relación materia y electricidad, faltaban las bases fundamentales de la combinación química explicada por Dalton en su teoría atómica. El modelo propuesto por Thomson consideraba al átomo como una esfera de masa cargada positivamente y sobre la cual flotan los electrones, exactamente como se encuentran las uvas, pasas o ciruelas sobre un pastel. Modelo Atómico de Ernest Rutherford: Rutherford, científico británico, nacido en Nueva Zelanda estudio de la radioactividad, descubierta a finales del s. XIX, había conducido a la hipótesis de que el número atómico representaba el número de unidades de carga positiva del átomo y, puesto que este es neutro, también el número de electrones. La naturaleza de las distintas radiaciones que emite el radio fue establecida por E. Rutherford en 1903 y, en 1911, el propio Rutherford inició una serie de experimentos cruciales de los que surgió el concepto de núcleo atómico. En estos experimentos, Rutherford y sus colaboradores H. Geiger y E. Marsden utilizaron una fuente de partículas y, mediante la interposición de planchas de plomo, colimaron el haz de partículas y lo dirigieron sobre una lámina de oro muy fina. Las partículas atravesaron la lámina e incidían sobre una superficie cubierta de sulfuro de zinc, provocando un centelleo. A partir de la observación de este centelleo era posible concluir que la gran mayoría de las partículas atravesaban las láminas sin sufrir, o casi sin sufrir, desviación, mientras que algunas sufrían una desviación considerable e incluso unas pocas no lograban atravesar la lámina, rebotando en ella como una pelota contra una pared. Este resultado contradecía el modelo atómico de Thomson, ya que, en caso de ser ese correcto, las partículas no deberían sufrir diferentes desviaciones. Para explicarlo, Rutherford supuso que toda la carga positiva del átomo estaba concentrada en una región, a la que se dio el nombre de núcleo, cuyo diámetro era una diezmilésima del diámetro del átomo. Los electrones, orbitando en torno al núcleo, equilibrarían la carga positiva de éste, que estaría representada por partículas denominadas protones, de carga igual y de signo contrario a la de los electrones. La materia está así practicamente vacía, lo que explica que la mayoría de las partículas que incidan en la lámina de oro no se desvíen, mientras que las partículas que pasan cerca del núcleo de un átomo de oro sufren fuertes desviaciones, y las que inciden directamente sobre un núcleo, rebotan. La casi totalidad de la masa del átomo correspondiente al núcleo, puesto que la masa del protón, según se había determinado experimentalmente, es 1836 veces mayor que la masa del electrón. Como se sabía que el número atómico representa el número de cargas positivas en el núcleo y puesto que el número de protones necesario para obtener las masas de los átomos era superior al número atómico, era preciso suponer que en el núcleo había, además de los protones que se neutralizaban mutuamente de manera que no <ejercían> como cargas, sino sólo aportando masa. Rutherford no se sentía satisfecho con la idea de que en el núcleo también hubiera electrones y en 1920 especuló con la posibilidad de que en el núcleo hubiera otras partículas de masaa similar al protón, pero carentes de carga eléctrica a las que, por esta razón, se denominó neutrones. La existencia de neutrones fue confirmada por J. Chadwick en 1932, cuando identificó como constituida por esas partículas netras la radiación obtenida al bombardear berilio con partículas . Modelo Atómico de Niels Bohr: Niels Bohr, físico danés. Para explicar la estructura del átomo, el físico danés Niels Bohr desarrolló en 1913 una hipótesis conocida como teoría atómica de Bohr. Bohr supuso que los electrones están dispuestos en capas definidas, o niveles cuánticos, a una distancia considerable del núcleo. La disposición de los electrones se denomina configuración electrónica. El número de electrones es igual al número atómico del átomo: el hidrógeno tiene un único electrón orbital, el helio dos y el uranio 92. Las capas electrónicas se superponen de forma regular hasta un máximo de siete, y cada una de ellas puede albergar un determinado número de electrones. La primera capa está completa cuando contiene dos electrones, en la segunda caben un máximo de ocho, y las capas sucesivas pueden contener cantidades cada vez mayores. Ningún átomo existente en la naturaleza tiene la séptima capa llena. Los “últimos” electrones, los más externos o los últimos en añadirse a la estructura del átomo, determinan el comportamiento químico del átomo. Todos los gases inertes o nobles (helio, neón, argón, criptón, xenón y radón) tienen llena su capa electrónica externa. No se combinan químicamente en la naturaleza, aunque los tres gases nobles más pesados (criptón, xenón y radón) pueden formar compuestos químicos en el laboratorio. Por otra parte, las capas exteriores de los elementos como litio, sodio o potasio sólo contienen un electrón. Estos elementos se combinan con facilidad con otros elementos (transfiriéndoles su electrón más externo) para formar numerosos compuestos químicos. De forma equivalente, a los elementos como el flúor, el cloro o el bromo sólo les falta un electrón para que su capa exterior esté completa. También se combinan con facilidad con otros elementos de los que obtienen electrones. Las capas atómicas no se llenan necesariamente de electrones de forma consecutiva. Los electrones de los primeros 18 elementos de la tabla periódica se añaden de forma regular, llenando cada capa al máximo antes de iniciar una nueva capa. A partir del elemento decimonoveno, el electrón más externo comienza una nueva capa antes de que se llene por completo la capa anterior. No obstante, se sigue manteniendo una regularidad, ya que los electrones llenan las capas sucesivas con una alternancia que se repite. El resultado es la repetición regular de las propiedades químicas de los átomos, que se corresponde con el orden de los elementos en la tabla periódica. Resulta cómodo visualizar los electrones que se desplazan alrededor del núcleo como si fueran planetas que giran en torno al Sol. No obstante, esta visión es mucho más sencilla que la que se mantiene actualmente. Ahora se sabe que es imposible determinar exactamente la posición de un electrón en el átomo sin perturbar su posición. Esta incertidumbre se expresa atribuyendo al átomo una forma de nube en la que la posición de un electrón se define según la probabilidad de encontrarlo a una distancia determinada del núcleo. Esta visión del átomo como “nube de probabilidad” ha sustituido al modelo de sistema solar. Mecánica ondulatoria: El físico francés Louis Victor de Broglie sugirió en 1924 que, puesto que las ondas electromagnéticas muestran algunas características corpusculares, las partículas también deberían presentar en algunos casos propiedades ondulatorias. Esta predicción fue verificada experimentalmente pocos años después por los físicos estadounidenses Clinton Davisson y Lester Halbert Germer y el físico británico George Paget Thomson, quienes mostraron que un haz de electrones dispersado por un cristal da lugar a una figura de difracción característica de una onda. El concepto ondulatorio de las partículas llevó al físico austriaco Erwin Schrödinger a desarrollar una `ecuación de onda' para describir las propiedades ondulatorias de una partícula y, más concretamente, el comportamiento ondulatorio del electrón en el átomo de hidrógeno. Aunque esta ecuación diferencial era continua y proporcionaba soluciones para todos los puntos del espacio, las soluciones permitidas de la ecuación estaban restringidas por ciertas condiciones expresadas por ecuaciones matemáticas llamadas funciones propias o eigenfunciones (del alemán eigen, `propio'). Así, la ecuación de onda de Schrödinger sólo tenía determinadas soluciones discretas; estas soluciones eran expresiones matemáticas en las que los números cuánticos aparecían como parámetros (los números cuánticos son números enteros introducidos en la física de partículas para indicar las magnitudes de determinadas cantidades características de las partículas o sistemas). La ecuación de Schrödinger se resolvió para el átomo de hidrógeno y dio resultados que encajaban sustancialmente con la teoría cuántica anterior. Además, tenía solución para el átomo de helio, que la teoría anterior no había logrado explicar de forma adecuada, y también en este caso concordaba con los datos experimentales. Las soluciones de la ecuación de Schrödinger también indicaban que no podía haber dos electrones que tuvieran sus cuatro números cuánticos iguales, esto es, que estuvieran en el mismo estado energético. Esta regla, que ya había sido establecida empíricamente por Wolfgang Pauli en 1925, se conoce como principio de exclusión. Louis Victor Broglie (1892-1987), físico y premio Nobel francés, que contribuyó de manera fundamental al desarrollo de la teoría cuántica. De Broglie nació en Dieppe y estudió en la Universidad de París. Trató de racionalizar la doble naturaleza de la materia y la energía, comprobando que las dos están compuestas de corpúsculos y tienen propiedades ondulatorias. Por su descubrimiento de la naturaleza ondulatoria de los electrones (1924), recibió el Premio Nobel de Física en 1929. Fue elegido miembro de la Academia de Ciencias (1933) y de la Academia Francesa (1943). Fue nombrado profesor de física teórica en la Universidad de París (1928), secretario permanente de la Academia de Ciencias (1942) y consejero de la Comisión de Energía Atómica Francesa (1945). Werner Karl Heisenberg (1901-1976), físico y Premio Nobel alemán, que desarrolló un sistema de mecánica cuántica y cuya indeterminación o principio de incertidumbre ha ejercido una profunda influencia en la física y en la filosofía del siglo XX. Heisenberg nació el 5 de diciembre de 1901 en Wurzburgo y estudió en la Universidad de Munich. En 1923 fue ayudante del físico alemán Max Born en la Universidad de Gotinga, y desde 1924 a 1927 obtuvo una beca de la Fundación Rockefeller para trabajar con el físico danés Niels Bohr en la Universidad de Copenhague. En 1927 fue nombrado profesor de física teórica en la Universidad de Leipzig. Después fue profesor en las universidades de Berlín (1941-1945), Gotinga (1946-1958) y Munich (1958-1976). En 1941 ocupó el cargo de director del Instituto Kaiser Wilhelm de Química Física (que en 1946 pasó a llamarse Instituto Max Planck de Física). Estuvo a cargo de la investigación científica del proyecto de la bomba atómica alemana durante la II Guerra Mundial. Bajo su dirección se intentó construir un reactor nuclear en el que la reacción en cadena se llevara a cabo con tanta rapidez que produjera una explosión, pero estos intentos no alcanzaron éxito. Estuvo preso en Inglaterra después de la guerra. Heisenberg, uno de los primeros físicos teóricos del mundo, realizó sus aportaciones más importantes en la teoría de la estructura atómica. En 1925 comenzó a desarrollar un sistema de mecánica cuántica, denominado mecánica matricial, en el que la formulación matemática se basaba en las frecuencias y amplitudes de las radiaciones absorbidas y emitidas por el átomo y en los niveles de energía del sistema atómico. El principio de incertidumbre desempeñó un importante papel en el desarrollo de la mecánica cuántica y en el progreso del pensamiento filosófico moderno. En 1932, Heisenberg fue galardonado con el Premio Nobel de Física. Erwin Schrödinger (1887-1961), físico y premio Nobel austriaco, conocido sobre todo por sus estudios matemáticos de la mecánica ondulatoria y sus aplicaciones a la estructura atómica. Nació en Viena y estudió en la universidad de esa ciudad. Dio clases de física en las universidades de Stuttgart (Alemania), Breslau (Polonia), Zurich, Berlín, Oxford y Graz (Austria). Desde 1940 hasta su jubilación en 1955 fue director de la escuela de física teórica del Instituto de Estudios Avanzados de Dublín. La aportación más importante de Schrödinger a la física fue el desarrollo de una rigurosa descripción matemática de las ondas estacionarias discretas que describen la distribución de los electrones dentro del átomo. Schrödinger demostró que su teoría, publicada en 1926, era el equivalente en matemáticas a las teorías de mecánica matricial que había formulado el año anterior el físico alemán Werner Heisenberg. Juntas, sus teorías constituyeron en buena medida la base de la mecánica cuántica. Schrödinger compartió en 1933 el Premio Nobel de Física con el británico Paul A. M. Dirac por su aportación al desarrollo de la mecánica cuántica. Su investigación incluía importantes estudios sobre los espectros atómicos, la termodinámica estadística y la mecánica ondulatoria. Modelos atómicos La evolución de los modelos físicos del átomo se vio impulsada por los datos experimentales. El modelo de Rutherford, en el que los electrones se mueven alrededor de un núcleo positivo muy denso, explicaba los resultados de experimentos de dispersión, pero no el motivo de que los átomos sólo emitan luz de determinadas longitudes de onda (emisión discreta). Bohr partió del modelo de Rutherford pero postuló además que los electrones sólo pueden moverse en determinadas órbitas; su modelo explicaba ciertas características de la emisión discreta del átomo de hidrógeno, pero fallaba en otros elementos. El modelo de Schrödinger, que no fija trayectorias determinadas para los electrones sino sólo la probabilidad de que se hallen en una zona, explica parcialmente los espectros de emisión de todos los elementos; sin embargo, a lo largo del siglo XX han sido necesarias nuevas mejoras del modelo para explicar otros fenómenos espectrales. Conclusión Dalton fue el primero que basándose en hechos experimentales construyó una teoría científica acerca de átomos. En ella, se postulaba la indivisibilidad atómica, idea que permitió el logro de resultados extraordinarios. Sin embargo, a fines del siglo XIX y a principios del siguiente, diversas experiencias sugirieron que el átomo era divisible, es decir, se hallaba constituido por otros corpúsculos. En efecto, J. Thomson observó que, en ocasiones, escapaban partículas cargadas con electricidad negativa a las que denominó electrones. A partir de ello, J. Thomson concibió el átomo como una esfera cargada positivamente en cuyo interior se hallaban electrones en movimiento. En 1910, E. Rutherford llegó a la conclusión de que la carga eléctrica positiva del átomo, la de mayor peso, estaba concentrada e un pequeño volumen que denomino núcleo, admitiendo que los electrones giraban alrededor del mismo. Cuatro años después, N. Bohr estableció un modelo atómico según el cual los electrones siguen trayectorias circulares y definidas alrededor del núcleo, que denominó órbitas, pudiendo saltar de una a otra órbita. En 1925, los estudios de W. Heisenberg y E. Schrödinger permitieron averiguar que no puede hablarse de órbita plenamente definidas, sino que únicamente cabe calcular la probabilidad de que un electrón se halle, en un cierto instante, en un lugar determinado.
Sí, se trata del Monte Olimpo (en latín Olympus Mons) Se encuentra en el planeta Marte, en las coordenadas aproximadas de 18º N, 226º E. Su naturaleza de montaña era conocida antes de que las sondas espaciales visitaran el planeta gracias a su albedo, siendo conocido por los astrónomos como Nix Olympica. Es la montaña y volcán mas grande del sistema solar. Se eleva 27 kilómetros sobre la llanura circundante, lo que equivale a tres veces la altura del monte Everest, y a 25 km sobre el nivel medio de la superficie marciana. - Encontrarás más información y una comparación con el Monte Everest Está flanqueado por grandes acantilados de hasta 6 km de altura, y su caldera tiene 85 km de largo, 60 km de ancho y 2,4-2,8 km de profundidad, pudiéndose apreciar hasta seis chimeneas superpuestas de cronología sucesiva. La base del volcán mide 600 km de diámetro incluyendo el borde exterior de los acantilados, lo cual le otorga una superficie en su base de 283.000 km² aproximadamente, lo que sería la superficie del Ecuador. Este volcan estan grande que una persona que estuviera en marte sería incapaz de ver si quiera la silueta del volcán, ni siquiera desde una distancia a la cual la curvatura del planeta empezara a ocultarla. El efecto por tanto sería el de estar contemplando una “pared”, o bien confundir la misma con la línea del horizonte. La única forma de ver la montaña adecuadamente es desde el espacio. Igualmente, si alguien se encontrara en la cima del volcán y mirase hacia abajo no podría ver el final, ya que la pendiente llegaría hasta el horizonte. Es un error pensar que la cima del Monte Olimpo está por encima de la atmósfera marciana. Olympus Mons es un volcán de escudo en forma de caldera. Las islas Hawai son un ejemplo de volcanes muy similares a menor escala, tal como el volcán Manua Loa, el mas grande del planeta. fuente: http://www.planetacurioso.com/2006/10/26/%C2%BFsabias-que-el-volcan-mas-grande-que-se-conozca-no-se-encuentra-en-la-tierra/
Hace casi 40 años, el 20 de julio de 1969, el astronauta norteamericano Neil Armstrong, frente a una audiencia estimada de mil millones de televidentes daba si pequeño paso, con el pie izquierdo, y se paraba sobre la polvorienta superficie de la Luna. La luz del Sol, sin una atmosfera que la difuminase, daba un brillo extraño a la escena. En ese momento comenzaba una nueva era para el hombre, y una nueva leyenda urbana. Es que no son pocos los que hoy piensan que todo se trato de un montaje. De hecho, según una encuesta encargada por la NASA, el 11% de los norteamericanos cree que en realidad el “alunizaje” se filmo en el desierto de Nevada, a solo 150 kilómetros de Las Vegas. La teoría del engaño, apoyada entre otros por los polémicos autores Bill Kaysing, Ralph René o Bart Winfield Sibrel, afirma que se monto un estudio de televisión en el desierto, y desde allí se trasmitieron las imágenes que el resto del mundo creyó provenían del Mar de la Tranquilidad, en la Luna. El objeto de dicho engaño habría sido cumplir, a cualquier precio, la promesa que, en plena guerra fría, había hecho el presidente Kennedy al Congreso de Estados Unidos. Kennedy se comprometía a situar un hombre en la Luna y devolverlo sano y salvo a la Tierra antes del fin de la década del sesenta. Esa era su respuesta al Sputnik ruso. Además, no debemos olvidar que en 1969 la Guerra de Vietnam se encontraba en pleno apogeo, por lo que un alunizaje constituiría una distracción muy conveniente para un gobierno que tenía en haber más de 50.000 muertos en una guerra cuyo sentido no estaba demasiado claro. Bill Kaysing, uno de los más férreos defensores de la teoría de la conspiración, trabajó entre 1956 y 1963 como redactor técnico en las misiones Apolo. "Durante este tiempo la NASA realizó un estudio de viabilidad que indicó que sólo tenían un 0,0017% de posibilidades de situar un hombre en la Luna y de devolverlo luego a Tierra.", dice Kaysing-, y asegura que es imposible que para 1969 hubiesen alcanzo un éxito del 100%. En realidad, la tecnología utilizada por el Apolo 11 era muy primitiva comparada con los estándares actuales, y según algunos, este hecho da la razón a Kaysing. El ordenador de a bordo tenía menos memoria que una lavadora moderna. Entre las objeciones que plantean los partidarios de la teoría conspirativa se encuentra la ausencia de estrellas en las fotos tomadas en la Luna por los tripulantes de las diversas misiones Apolo. De hecho, la cuestión tiene cierta lógica: el cielo de la Luna es límpido, y no hay atmosfera que entorpezca la visión del espacio, así que ¿dónde están las estrellas? La respuesta a esa pregunta es bastante simple: las estrellas están ahí, solo que no podemos verlas. Se trata de objetos cuyo brillo es demasiado tenue para aparecer sobre la fotografía. En realidad, para sacar la foto de un astronauta vestido con un traje blanco sobre el fondo negro del espacio hay que ajustar la cámara de forma que el tiempo de exposición sea lo suficientemente pequeño para semejante contraste. Las estrellas simplemente no alcanzan a registrarse sobre la película. A algunos le resulta extraño a ninguno de los astronautas se le ocurriese hacer una instantánea con un tiempo de exposición suficiente para capturar el firmamento tachonado de estrellas. La cámara Hasselblad con película Ektachrome de 160 ASA hubiese podido tomar una esplendida foto del cielo. Los escépticos argumentan que tal foto no se tomo por ese cielo hubiese sido imposible de reproducir sin despertar las sospechas de los astrónomos. Una empresa de publicidad llamada The Viral Factory publicó un vídeo en internet (el año 2002) que cuestionaba el alunizaje del Apolo. En él se veía como uno de los astronautas (Neil Armstrong) abandona el Apolo 11 para pisar el suelo lunar. En ese mismo instante uno de los focos de la escenografía se caía. Se veía como de inmediato ingresaban al set una serie de técnicos para arreglar el desperfecto y seguir con la grabación. Para rematar, de fondo se escuchaba la supuesta comunicación de los astronautas con el centro de control de misión. Este video fue presentado en sitio www.moontruth.com , y puedes verlo aquí. link: http://www.youtube.com/watch?v=RS_Oy5aASM4 Según moontruth.com, el video provenía de productores de televisión cercanos a la NASA. A pesar de que casi todos los expertos aseguran de que se trata de un “spoof" los responsables del sitio siguen sosteniendo la autenticidad del vídeo. Otro argumento esgrimido a menudo es el porqué la bandera estadounidense ondea en uno de los vídeos. Como no hay viento en la Luna, esto no debería ocurrir. Sin embargo, tal como puede verse en muchas fotografías, la bandera tenía un soporte en su parte superior para que permaneciera extendida. Las arrugas y ondulaciones producidas por haber estado legada durante el viaje le da una apariencia que puede confundirse con la de una bandera ondeando, pero en realidad, los videos muestran como se queda completamente inmóvil luego de que los astronautas la colocan sobre la Luna. También se sostiene que es imposible tomar miles de fotografías, todas ellas perfectamente expuestas y enfocadas. La principal prueba en contra de este argumento son, justamente, los cientos de fotografías que están desenfocadas, o incluso, veladas. Se dice que el brillo de la bandera y las palabras “United States” siempre está presente, aún cuando todo es oscuro alrededor. Ninguna de la fotografías coincide con las tomas de video, aunque la NASA asegura que las tomó al mismo tiempo. La explicación a este fenómeno hay que buscarla en los reflejos. La superficie lunar refleja una buena parte de la luz del Sol, iluminando partes del módulo, construido de material a su vez reflectante. No es cierto que las fotografías no coincidan con los vídeos grabados. De hecho, científicos y geólogos de todo el mundo las han analizado durante décadas, sin hallar ninguna cosa extraña. Si te cruzas con un fanático de las conspiraciones, seguramente te dirá que el espacio exterior está plagado de mortales radiaciones emitidas por el sol, que, extrañamente, no dañaron a ningún astronauta. Ninguno contrajo cáncer, ni siquiera los de la misión Apolo 16 quienes fueron sorprendidos por una llamarada solar que debió haberlos matado. Pero en realidad, no hay pruebas de que hubiera una erupción solar importante durante el vuelo del Apolo 16. Hubo varias mese después de que la misión hubiese terminado, en agosto de 1972. La actitud de” ¡Si no lo veo no lo creo!” es propia de los partidarios de las conspiraciones. Sin embargo, cuando una nave tripulada como el Apolo 11 realiza un viaje por el espacio permanece en contacto radioeléctrico con la estaciones de seguimiento en tierra. En ese caso, estaban en California, Australia y España (Fresnedillas, cerca de Madrid), cubriendo cada una ocho horas del día. Medían la velocidad de la nave, su posición y comprobaban que no se apartara de su órbita. No eran datos secretos, sino todo lo contrario. Cualquier particular equipado con un radiotelescopio podría “oír” al Apolo. Incluso los rusos seguían a las naves americanas. Si todo hubiera sido un fraude, hubiesen sido precisamente los soviéticos quienes lo hubiesen denunciado. La llegada del Apolo a la Luna fue una gran derrota para el régimen soviético. La cuestión es que, gracias a la publicación de algunos libros sobre el tema, y a un análisis demasiado superficial de la información disponible (sobre todo de las fotografías), un gran porcentaje de los propios norteamericanos ponen en duda la veracidad de las misiones lunares. Sin embargo, no dudan en aceptar, por ejemplo, incidentes como de Roswell. Fuente: http://www.neoteo.com/la-llegada-del-hombre-a-la-luna-fraude-o-realidad.neo
La Argentina es un destino turístico que atrae por las abundantes y muy variadas bellezas naturales, sus costumbres y gastronomías típicas. La infraestructura turística es buena. Este territorio es vasto y se extiende desde las más elevadas cumbres de los Andes en el oeste hacia los grandes ríos y las extensísimas playas y acantilados del Mar Argentino en el este; desde la selva tropical al norte hasta los valles, glaciares, lagos y bosques fríos de la Patagonia Andina en el sur siendo la principal y más atractiva puerta de ingreso a la Antártida. Las grandes distancias se recorren en avión, aunque también es posible hacerlo por tierra, en transporte público de larga distancia. Conviene tener en cuenta los aspectos climáticos y estacionales de Argentina, predomina un clima templado, aunque -dada la extensión- en el sur y en las zonas montañosas elevadas (incluso las tropicales) las temperaturas son frecuentemente frías y ocurren nevadas; complementariamente, en las zonas bajas del norte las temperaturas son cálidas. Los meses más fríos son los de mayo, julio y junio; los meses más cálidos son los de diciembre, enero y febrero. Según cifras oficiales de la Organización Mundial del Turismo, en 2007 el país recibió a más de 4.600.000 turistas extranjeros, lo que significó unos 4.300 millones de dólares de ingreso de divisas. La Argentina es el segundo país más visitado de América del Sur (detrás de Brasil) y el quinto más visitado del continente americano. Los turistas extranjeros provienen principalmente de Brasil, Chile, Perú, Colombia, México, Bolivia, Ecuador, Uruguay, Venezuela y Paraguay y los europeos de España, Italia, Francia, Alemania, Reino Unido y Suiza. En los últimos años, revistas especializadas en turismo recomendaron visitar a la Argentina, como hizo Lonely Planet, que en 2006 la distinguió con el primer puesto como el mejor destino turístico a nivel mundial, destacando la variedad de los paisajes naturales, la gastronomía y la seguridad para el turista. Destinos principales: Ciudad de Buenos Aires, alguna vez considerada, debido principalmente a la arquitectura, la "París del Hemisferio Sur" por varios viajeros, ofrece una amplia actividad cultural. Los viajeros eligen generalmente una visita nocturna a los locales donde se baila tango y un paseo a una típica estancia (en la provincia de Buenos Aires), para degustar el tradicional asado. En los últimos años, surgieron nuevos circuitos temáticos, entre ellos muchos dedicados a personalidades importantes como Carlos Gardel, Eva Perón o Jorge Luis Borges. También dispone de numerosos paseos de compras (shoppings), entre los cuales se destacan el Alto Palermo, Paseo Alcorta, Patio Bullrich, Abasto de Buenos Aires y Galerías Pacífico. Cataratas del Iguazú. Cataratas del Iguazú, ubicadas al noreste, zona de selva subtropical, son las cataratas de agua más conocidas de toda la región y su explotación turística cuenta con buen desarrollo de infraestructura, y con paseos muy diversos. Es zona de Parque Nacional, donde se preservan la flora y fauna originales. Su salto más imponente es la llamada Garganta del Diablo. Otros importantes son los llamados Dos Hermanas, Bossetti o Álvar Núñez, en homenaje a su descubridor, Álvar Núñez Cabeza de Vaca. Tren de las Nubes, este peculiar paseo en tren por la zona de la Puna, una altiplanicie casi desértica, con enormes contrastes en su recorrido, que va subiendo las laderas de los Andes, ubicada en la provincia de Salta. Se interrumpió momentáneamente su servicio en julio de 2005 por reparaciones, teniéndose programada su reactivación a la brevedad.( Según las últimas noticias, estaría en marcha en Julio 2009 con un viaje los sábados) Actualmente, el destino final es la ciudad de San Antonio de los Cobres. Costanera de Rosario. Glaciar Perito Moreno, formando parte del Campo de Hielo Sur es un inmenso glaciar que divide en dos el lago Argentino y cíclicamente lo bloquea hasta que se produce la ruptura del tapón de hielo. Está ubicado cerca de El Calafate, una pequeña ciudad patagónica. En cualquier época del año se producen continuos desprendimientos de enormes bloques de hielo, lo que es un espectáculo natural. Este glaciar como sus vecinos se encuentra enmarcado por un majestuoso paisaje de abruptas montañas como el Chaltén y grandes lagos. Bariloche, Villa La Angostura, San Martín de los Andes, Junín de los Andes, El Bolsón, Esquel, Trevelín, Los Antiguos, Copahue, Caviahue, en zonas de montañas cubiertas del hermoso bosque andino patagónico y lagos glaciarios, con los atractivos adicionales de la pesca y centros de deportes invernales. Glaciar en el Canal de Beagle, Tierra del Fuego. Ushuaia, la ciudad más austral del mundo, en Tierra del Fuego, destino típico del extremo sur del país, atrae a los visitantes con una muy importante oferta turística con excursiones, gastronomía y la sensación de estar, literalmente, en el fin del mundo. Al norte de la isla, la ciudad de Río Grande resulta atractiva por su antiguo barrio de casas de madera pintadas varia y sutilmente o por la excelente pesca de truchas. Más al sur, es famoso el ferrocarril que parte de Ushuaia y llega hasta el Parque Nacional Tierra del Fuego, junto a la bahía de Lapataia. Se ofrecen además cruceros por el canal Beagle, observando colonias de lobos marinos, y una visita al Faro Les Eclareurs, al bello Lago Fagnano (o Kami) o a la casi inaccesible Isla de los Estados en donde se encuentra el Faro del Fin del Mundo, el paisaje de los bosques fueguinos toma un aspecto casi mágico durante los otoños australes al cubrirse de colores rojizos los follajes de los densos bosques. Zona del Patio Olmos de Córdoba, comienzo de Nueva Córdoba. Sierras de Córdoba, de ameno clima y paisajes que varían entre lo bucólico y lo agreste, allí los principales centros turísticos son: Villa General Belgrano y La Cumbrecita, poblaciones turísticas con gran influencia centroeuropea en las Sierras de Córdoba. Otras ciudades importantes son Carlos Paz, Cosquín, La Falda, Mina Clavero o el gran lago salado de Mar Chiquita. La Ciudad de Córdoba posee asimismo un gran atractivo turístico, especialmente en su valiosa edificación del período colonial o en sus paisajes urbanos. Presenta también una muy buena infraestructura turística con importantes hoteles 5 estrellas, centros comerciales de alto nivel, como así también resalta en el ámbito de la gastronomía y la diversión. La ciudad de Córdoba es una de las más pintorescas de la Argentina ya que presenta un centro histórico con bella arquitectura barroca colonial mezclada con los altos edificios modernos lo que le dan a la ciudad un gran atractivo turístico. Ischigualasto-Valle de la Luna. Ischigualasto, o "Valle de la Luna" también denominado, ofrece un extraño paisaje, donde la escasez de vegetación y la más variada gama de colores de sus suelos, más el capricho en las formas de rocas y de los montes, lo hacen ser un lugar predilecto para turistas, tanto nacionales como extranjeros. Este parque provincial fue declarado [[Anexoatrimonio de la Humanidad en América Latina y el Caribe Fuente: http://es.wikipedia.org/wiki/Turismo_en_Argentina