Mucho se ha descrito sobre el uso de energias renovables, las mas conocidas son la energia eolica, la energia solar, la energia quimica, energia cinetica.
Pero existen otros tipos de energía renovable que no han sido aprovechados, estoy hablando de la posibilidad e utilizar la capacidad de la clorofila para producir glucosa (carbono) en base a la formula de la fotosíntesis,
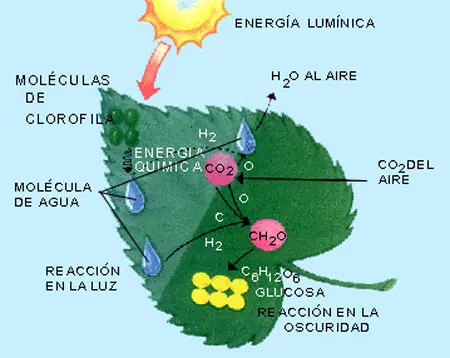
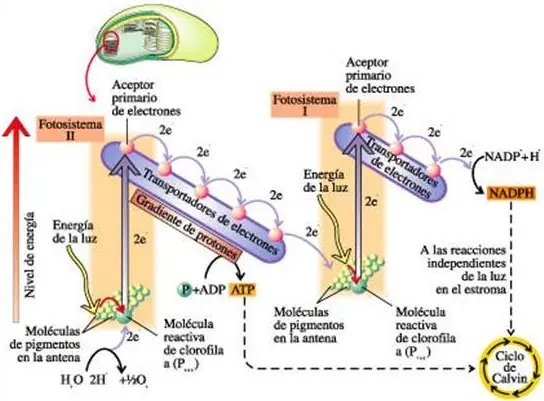
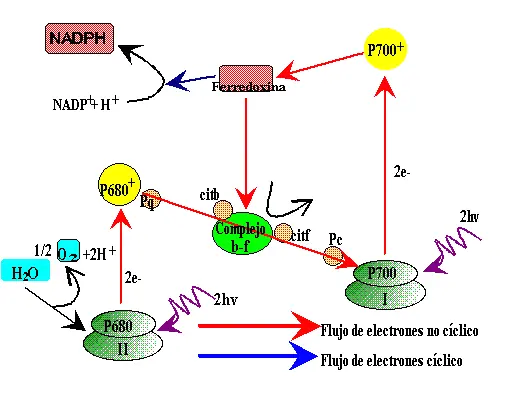
pero excluyendo el uso en si de plantas, un tipo de fotosíntesis sintética, que aglomere la cantidad de moléculas necesarias para la producción de glucosa, lamentablemente las investigaciones se contrapone a los intereses de las grandes empresas del petroleo.
Plantas C4
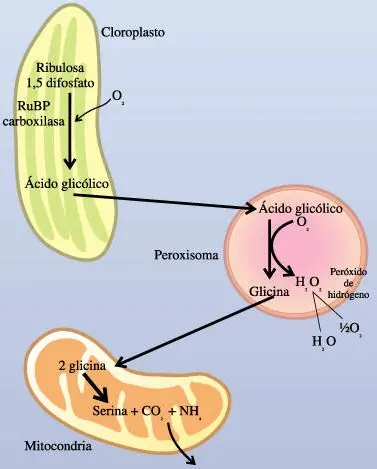
Las Plantas C4 tiene una peculiaridad que no tiene ninguna otra planta, necesitan poca o nula cantidad de agua para la produccion de energia (Carbono)
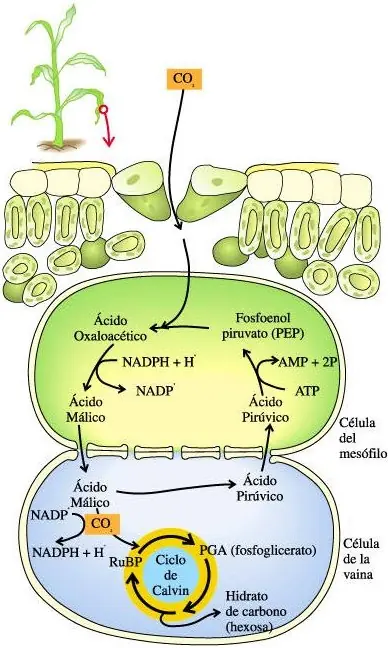
Y no solo producen carbono, si no que producen Agua!
Existen tambien la posibiidad de obtener energia quimica utilizando todo el potencial de la energia libre de Formacion de una molecula:
La espontaneidad química es la capacidad de una reacción química de evolucionar desde un reactivo o conjunto de reactivos hacia la obtención de producto o conjunto de productos para determinadas condiciones (presión, temperatura, concentraciones de productos y reactivos, etc.).
Dicho fenómeno se define mediante la siguiente expresión que relaciona las tres funciones termodinámicas:
ΔG° = ΔH°-TΔS°
Siendo: ΔG° la variación de la energía libre de Gibbs en condiciones estándar; ΔH° la variación de la Entalpía en condiciones estándar; T la temperatura absoluta (Kelvin) y ΔS° la variación de la Entropía en condiciones estándar. Dichas condiciones estándar corresponden a reacciones llevadas acabo a 298 K, 1 Atm y reactivos en concentraciones 1 M en sus fases más estables.
En base a la ecuación de ΔG° se concluye: si ΔG° es menor que 0 la reacción es espontánea (exergónica) con la variación entrópica (ΔS°) y la temperatura (T) dadas. Si en cambio, es mayor que 0 no es espontánea (endergónica), por lo que se deberá aumentar la temperatura del sistema o realizar trabajo (W) sobre el mismo, es decir, suministrar energía para que la reacción ocurra.
Cabe destacar que la función ΔG (en condiciones diferentes de la estándar) solo es criterio de espontaneidad cuando el trabajo distinto del de expansión (W') es cero.
Pero existen otros tipos de energía renovable que no han sido aprovechados, estoy hablando de la posibilidad e utilizar la capacidad de la clorofila para producir glucosa (carbono) en base a la formula de la fotosíntesis,



pero excluyendo el uso en si de plantas, un tipo de fotosíntesis sintética, que aglomere la cantidad de moléculas necesarias para la producción de glucosa, lamentablemente las investigaciones se contrapone a los intereses de las grandes empresas del petroleo.
Plantas C4
Las Plantas C4 tiene una peculiaridad que no tiene ninguna otra planta, necesitan poca o nula cantidad de agua para la produccion de energia (Carbono)

Y no solo producen carbono, si no que producen Agua!

Existen tambien la posibiidad de obtener energia quimica utilizando todo el potencial de la energia libre de Formacion de una molecula:
La espontaneidad química es la capacidad de una reacción química de evolucionar desde un reactivo o conjunto de reactivos hacia la obtención de producto o conjunto de productos para determinadas condiciones (presión, temperatura, concentraciones de productos y reactivos, etc.).
Dicho fenómeno se define mediante la siguiente expresión que relaciona las tres funciones termodinámicas:
ΔG° = ΔH°-TΔS°
Siendo: ΔG° la variación de la energía libre de Gibbs en condiciones estándar; ΔH° la variación de la Entalpía en condiciones estándar; T la temperatura absoluta (Kelvin) y ΔS° la variación de la Entropía en condiciones estándar. Dichas condiciones estándar corresponden a reacciones llevadas acabo a 298 K, 1 Atm y reactivos en concentraciones 1 M en sus fases más estables.
En base a la ecuación de ΔG° se concluye: si ΔG° es menor que 0 la reacción es espontánea (exergónica) con la variación entrópica (ΔS°) y la temperatura (T) dadas. Si en cambio, es mayor que 0 no es espontánea (endergónica), por lo que se deberá aumentar la temperatura del sistema o realizar trabajo (W) sobre el mismo, es decir, suministrar energía para que la reacción ocurra.
Cabe destacar que la función ΔG (en condiciones diferentes de la estándar) solo es criterio de espontaneidad cuando el trabajo distinto del de expansión (W') es cero.